文章信息
文章题目:Assembly and activation of EBV latent membrane protein 1
期刊:Cell
发表时间:2024年7月11日
主要内容:中国科学院生物物理所高璞、高光侠、张立国合作团队,在Cell 杂志上发表了文章Assembly and activation of EBV latent membrane protein 1,该研究发现LMP1 以一种全新且与此前猜测完全不同的机制进行寡聚自组装,并通过巧妙方式高效招募下游因子,从而激活和维持致病信号活化。另外,研究中发现的新机制和新界面,也为此前一些不清楚的现象提供了精确解释,并有望直接助力LMP1 靶向干预策略的开发。
原文链接:https://doi.org/10.1016/j.cell.2024.06.021
使用TransGen产品:
Trans10 Chemically Competent Cell (CD101)

研究背景
EBV(Epstein-Barr Virus)是一种人类疱疹病毒,也是首个报道的人类肿瘤病毒,全球约95% 的成人经历过感染并终生携带EBV。虽然通常不产生严重症状,但EBV 感染也有几率导致多种淋巴癌和上皮细胞癌,如鼻咽癌、霍奇金淋巴癌、伯基特淋巴癌、胃癌等。
潜伏期膜蛋白1(Latent Membrane Protein 1, LMP1)是EBV 编码的关键致癌蛋白。1985年,Elliott Kieff 课题组首次报道LMP1 单一蛋白表达即能诱发B 细胞的永生化,后续研究也相继发现LMP1 通过模拟CD40 信号参与B 细胞和上皮细胞增殖和早期癌变。而与CD40 不同,LMP1 信号的激活不依赖任何配体,且LMP1 介导的信号强度显著强于CD40。除了介导细胞转化和永生化,LMP1 还参与调控多种重要生命活动,如免疫应答、细胞因子和趋化因子分泌、细胞凋亡、细胞迁移、细胞互作、肿瘤侵袭和转移等。鉴于LMP1 与EBV 致病的高度关联性,以及LMP1 在EBV 相关恶性肿瘤中的广泛表达和分布,LMP1 一直被认为是EBV 阳性肿瘤鉴别诊断和靶向治疗的理想靶点。尽管目前对LMP1 介导的下游功能有了较多认识,然而作为产生多样性功能的核心前提—即LMP1 如何实现配体不依赖的组装和激活,仍然是困扰领域近40 年的难题,也是影响LMP1 靶向干预策略成功开发的重要阻碍。
文章概述
研究人员首先利用共聚焦显微镜进行细胞成像,发现LMP1 在生理表达水平下会在膜上呈现为明显的聚集形态。进一步的超分辨成像表明,LMP1 的聚集是一种宽度较为固定但长度不均一的细条状结构。这些结果表明LMP1 可在膜上组装成有趣的聚集,但其分子层面的细节仍不清楚。为辅助结构解析,研究人员进一步开展了系统性LMP1 抗体筛选,获得了能够稳定结合LMP1 跨膜区的鼠源单抗。通过抗体辅助策略,研究人员成功解析了LMP1 两种意想不到的聚集态结构:轴对称二聚体和filament 状高聚体。LMP1 单体以一种全新的方式进行跨膜区折叠,进而通过反向平行叠合形成稳定的二聚体结构;LMP1 二聚体是其进行更高级组装的基本单元,多个二聚体以“side-by-side”方式自组装形成filament 状高聚结构。重要的是,这些高分辨率的结构信息,恰好符合活细胞成像所观测到的独特聚集形态,从而在不同分辨率尺度上揭示了LMP1 的膜上聚集机制。
为进一步明确LMP1 的功能形式,研究人员对二聚体和寡聚体界面分别进行了系统突变,发现其均会破坏LMP1 在活细胞中的膜聚集形态,且均能阻断下游信号通路活化。这既证明了LMP1 分子间互作的重要性,也明确了LMP1 的寡聚filament 结构才是其真正的激活状态。超分辨成像结果表明,LMP1 在膜上的自发filament 状聚集可包含几十至数百个LMP1 二聚体单元。LMP1 的这种聚集在很低蛋白水平下即可发生,且随着LMP1 含量增加,多聚体的数量、强度和长度均呈现显著增长。这也是首次在较低表达水平下(类似病毒感染的表达水平),系统性观察到LMP1 在膜上的超分辨动态聚集和组装。
有趣的是,作为LMP1 的功能相关蛋白,宿主膜受体CD40 的激活需依赖其配体介导的三聚体组装;而且,LMP1 和CD40 共同的下游信号因子TRAF 蛋白,也是以三聚体形式发挥功能。因此,长期以来领域里普遍推测LMP1 也应该是采用三聚体的方式来组装,这样才能更好的与下游因子进行衔接。而LMP1 却是以二聚体为单元进行“side-by-side”方式的filament 自组装,那么其是如何有效协调信号转导的呢?研究人员通过细致分析,发现二聚体单元中的两个LMP1 的C 端,可以和邻近二聚体中一个LMP1 的C 端,在空间上呈现近似等边三角行的巧妙排列。由于C 端延伸的水溶区负责招募下游因子,因此这种filament 自组装方式,结构上等价于多个LMP1“三聚体”平行密集排列,从而能够比CD40 更高效招募下游因子和进行信号转导。研究人员也通过生化手段在体外重组了LMP1 与TRAF 复合体,利用电镜直接观察到LMP1 的filament 聚集确实可以同时招募多对TRAF 三聚体。LMP1 这种多位点且组成性的下游蛋白招募、激活方式,极大促进了信号转导强度,并有效维系了持续的增殖、癌变信号。
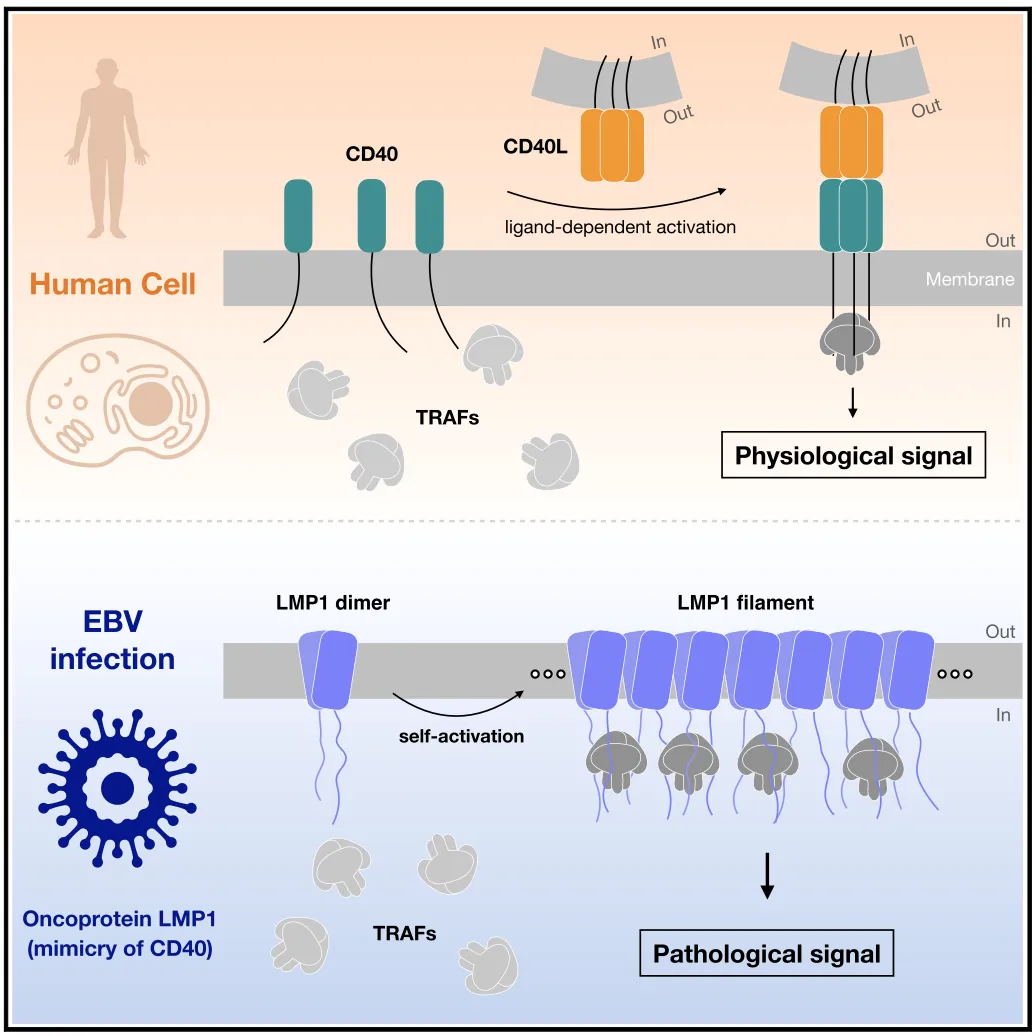
CD40 与LMP1 的不同激活机制
综上所述,该研究报道了EBV 关键致癌蛋白LMP1 自组装和组成性激活的分子基础,为EBV-LMP1 诱发致癌信号和调节免疫应答等生物学功能提供了新的理论模型。另外,该研究也为开发针对EBV 相关疾病的干预手段提供了新思路。
全式金生物产品支撑
优质的试剂是科学研究的利器。全式金生物的克隆感受态细胞产品CD101 Trans10 Chemically Competent Cell (CD101)助力本研究。
Trans10 Chemically Competent Cell (CD101)
Trans10化学感受态细胞经特殊工艺制作,可用于DNA 的化学转化。使用pUC19 质粒DNA 检测,转化效率可达108 cfu/μg DNA 以上。细胞具有硫酸链霉素 (StrR) 抗性。
产品特点
• 用于蓝、白斑筛选
• 适用于高效的DNA 克隆和质粒扩增,能保证高拷贝质粒的稳定复制
全式金生物产品再一次登上Cell 期刊,证明了大家对全式金生物产品品质和实力的认可,也完美诠释了全式金生物一直以来秉承的“品质高于一切,精品服务客户”的理念。全式金生物始终在助力科研的道路上砥砺前行,希望未来能与更多的科研工作者并肩奋斗,用更多更好的产品持续助力科研。
使用Trans10 Chemically Competent Cell产品发表的部分文章:
• Huang J, Zhang X, Nie X ,et al. Assembly and activation of EBV latent membrane protein 1[J]. Cell, 2024.(IF 45.5).
• Yao H, Song Y, Chen Y, et al. Molecular architecture of the SARS-CoV-2 virus[J]. Cell, 2020.(IF 45.5).
• Wang X, Xuan Y, Han Y, et al. Regulation of HIV-1 Gag-Pol expression by shiftless, an inhibitor of programmed-1 ribosomal frameshifting[J]. Cell, 2019.(IF 45.5).
• Zhong S, Zhang S, Fan X, et al. A single-cell RNA-seq survey of the developmental landscape of the human prefrontal cortex[J]. Nature, 2018.(IF 50.5).





